Cálculo de la potencia de la lente intraocular
El objetivo de una precisa cálculo de la potencia de la lente intraocular es proporcionar un lente intraocular (IOL) que ajustes específicos de los necesidades y deseos del paciente individual. El desarrollo de mejores instrumentos para medir la ojode longitud axial (AL) y el uso de fórmulas matemáticas más precisas para realizar los cálculos apropiados han mejorado significativamente la precisión con la que el cirujano determina el poder IOL.
Con el fin de determinar la potencia de la lente intraocular varios valores necesitan ser conocida:
- Longitud axial del ojo (AL)
- Corneal energía (K)
- Posición postoperatoria IOL dentro del ojo conocida como posición estimada (ELP)
- La constante de la cámara anterior: A constante u otra lente constante relacionado
De estos parámetros se miden los dos primeros antes de la implantación, el tercer parámetro, el ELP, deben calcularse matemáticamente antes de la implantación y el último parámetro es proporcionado por el fabricante de la lente intraocular.
Contenido
- 1 Longitud axial
- 1.1 Sonografía
- 1.2 Interferometría coherencia parcial
- 2 Energía córnea
- 3 Fórmulas de cálculo de potencia IOL
- 4 A-constant
- 5 Cálculo de la potencia de la lente intraocular después de la cirugía refractiva
- 6 Véase también
- 7 Referencias
- 8 Enlaces externos
Longitud axial
La longitud axial (AL) es la distancia entre la superficie anterior de la córnea y el fóvea y generalmente medido por A-scan. sonografía o biometría de coherencia óptica. AL es el factor más importante en el cálculo de lio: un error de 1 mm en AL medida resulta en un error refractivo de aproximadamente 2,35 D en un ojo promedio.[1]
Sonografía
En biometría de ultrasonido A-scan, un cristal oscila para generar una onda de sonido de alta frecuencia que penetra en el ojo. Cuando la onda de sonido se encuentra con una interfaz de los medios de comunicación, parte de la onda sonora se refleja hacia atrás, hacia la punta de prueba. Esos ecos permiten calcular la distancia entre la sonda y diversas estructuras en el ojo. Ultrasonografía no mide la distancia pero prefiero el tiempo requerido para que un pulso de sonido viajar de la córnea para el retina. La velocidad del sonido varía en diferentes partes del ojo. El ojo se divide ultrasonographically en cuatro componentes: córnea, cámara Anterior, espesor de la lente y cavidad vítrea. La velocidad del sonido en estos compartimientos son 1620, 1532, 1641, 1532 m/s respectivamente.[2] A través de los ojos normales se acepta una velocidad promedio de 1555 m/s para el cálculo. Instrumentos modernos utilizan velocidades de sonido separadas para los componentes de ojos de diferente para obtener la longitud axial total. El tiempo de tránsito medido se convierte en una distancia utilizando la fórmula d = t/v donde d es la distancia, t es el tiempo y v es la velocidad.[1]
Dos tipos de biometría de ultrasonido A-scan están actualmente en uso. La primera es contacto applanation biometría. Esta técnica requiere colocar una sonda de ultrasonido en la córnea central. Aunque esta es una manera conveniente para determinar la longitud axial para ojos más normales, errores en la medición casi invariablemente el resultado de la sonda aplicar sangría a la córnea y shallowing del compartimiento anterior. Puesto que el error de compresión es variable, eso no se puede compensar por una constante. IOL potencia calculado usando estas medidas llevarán a una sobreestimación de la potencia IOL. Los ojos más corto, este efecto se amplifica. El segundo tipo es biometría de inmersión A-scan, que requiere colocando una solución salina llena escleral cáscara entre la sonda y el ojo. Puesto que la sonda no ejerce presión directa sobre la córnea, se evita la compresión de la cámara anterior. Un acortamiento medio de 0.25-0.33 mm se ha divulgado entre mediciones de longitud axial de aplanación e inmersión, que se traducen en un error de la energía IOL por aproximadamente 1 D. En general, la biometría inmersión ha demostrado ser más precisa que la biometría applanation contacto en varios estudios. La principal limitación con el ultrasonido A-scan es la resolución de imagen pobre debido al uso de una longitud de onda relativamente larga y baja resolución (10 MHz) para medir una distancia relativamente corta. Además, las variaciones en el espesor retiniano alrededor de la fóvea contribuyen a la inconsistencia en la medición final.[3]
Interferometría coherencia parcial
La técnica de coherencia parcial interferometría mide el tiempo requerido para que luz infrarroja viajar a la retina. Porque la luz viaja a una velocidad demasiado alta para ser medido directamente, metodología de interferencia de la luz se utiliza para determinar el tiempo de tránsito y por lo tanto AL. Esta técnica no requiere contacto con el mundo, así se eliminan los artefactos de compresión corneal. Comparado con sonografía, la interferometría parcial coherencia proporciona medición AL más precisa y reproducible. Sin embargo, es difícil obtener una medida en presencia de una densa catarata u otras opacidades de los medios de comunicación, que limita el uso de esta técnica.
Otra ventaja del PCI sobre biometría de ultrasonido es que la medición de la longitud axial se realiza a través del eje visual ya que la paciente se le pide a fijar en el foco del láser. En altamente miope o staphylomatous los ojos, esto puede ser particularmente ventajoso ya que a veces puede ser difícil de medir la longitud axial verdadera a través del eje visual con una sonda de ultrasonido. También es superior a la ecografía en la medición del PCI pseudophakic y los ojos llenos de aceite de silicona. Para la biometría óptica, no es tan crítico como cambian los medios de comunicación porque la corrección del factor debe ser aplicado es mucho menor que en biometría de ultrasonido.[3] Cabe señalar que la longitud axial obtenida PCI puede ser ligeramente más larga que el que obtiene de ultrasonido. Esto es debido a PCI midiendo la distancia entre la superficie de la córnea y el RPE mientras las medidas de ultrasonido a la superficie anterior de la retina. Por lo tanto, muchas máquinas de medición de IOL requieren constantes IOL refinadas exclusivos de su mecanismo.
Energía córnea
El poder corneal central es el segundo factor más importante en la fórmula de cálculo. Para simplificar el cálculo, la córnea se asume que es una lente esférica delgada con una proporción fija curvatura corneal anterior a posterior y un índice de refracción de 1.3375. Poder corneal central puede medirse por keratometry o Topografía corneal. Córnea radio de curvatura se relaciona con la energía córnea con la ecuación: r = 337,5/K.[3]
Fórmulas de cálculo de potencia IOL
Cálculo de la potencia de la lente intraocular fórmulas se dividen en dos categorías principales: teóricas fórmulas y fórmulas de regresión. Fórmulas de regresión ahora son obsoletas y fórmulas teóricas modernas se utilizan en su lugar.[4] Las fórmulas de regresión son fórmulas empíricas generadas por un promedio de gran número de resultados clínicos postoperatorios (es decir, del análisis retrospectivo informático de los datos obtenidos de un grande muchos pacientes sometidos a cirugía). Las fórmulas de regresión más comunes son el SRK y SRK II. En la década de 1980 SRK y SRK II eran populares porque eran fáciles de usar. Sin embargo, error de energía a menudo resultó del uso de estas fórmulas.
La fórmula SRK se calcula fácilmente a mano como  , donde
, donde  es el poder IOL para ser utilizado para el emmetropia,
es el poder IOL para ser utilizado para el emmetropia,  el IOL específico, es una constante,
el IOL específico, es una constante, 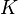 es la potencia media de refracción corneal (dioptrías), y
es la potencia media de refracción corneal (dioptrías), y  es la longitud del ojo (mm). La fórmula SRK II ajusta la constante A utilizar dependiendo de la longitud axial: aumentando la constante A para ojos cortos y disminuyendo la constante A para ojos largas.
es la longitud del ojo (mm). La fórmula SRK II ajusta la constante A utilizar dependiendo de la longitud axial: aumentando la constante A para ojos cortos y disminuyendo la constante A para ojos largas.
Fórmulas teóricas se basan en la óptica geométrica. El ojo es considerado un dos lente sistema (IOL y córnea) y la distancia prevista entre ellos que se llama la posición estimada lente (ELP) se utiliza para calcular la potencia de la lente. Todas las fórmulas requieren una estimación de la posición que el lio se sentará en el ojo, un factor conocido como el portfolio, que se define como la distancia entre la córnea y la lio. ELP se correlaciona con la colocación de la lente dentro del ojo, si es en el compartimiento anterior en el surco o en la bolsa capsular. También varía con configuración del implante y la ubicación de su centro óptico. Por ejemplo el uso de una lente menisco pide un valor menor de ELP que un IOL biconvexo.
Las fórmulas de cálculo de lio difieren en la forma calculan ELP. En la original fórmula teórica el PEL se considera un valor constante de 4 mm para cada objetivo en cada paciente.[4] Mejores resultados se obtienen relacionando el ELP esperado a la longitud axial y la curvatura corneal. Fórmulas teóricas modernas predicen ELP diferente basado en la longitud axial y poder corneal: ELP disminuye en los ojos más cortos y planas córneas y aumenta en los ojos más y más pronunciadas córneas. Las mejoras en el cálculo de la potencia IOL son el resultado de las mejoras en la previsibilidad del portfolio.[2]
Las fórmulas modernas más conocidas son SRK-T, Holladay 1, 2 Holladay, Hoffer-Q y Haigis. Estas fórmulas están programadas en el IOLMaster, Lenstar y más modernos instrumentos ultrasonographic, eliminando así la necesidad de utilizar fórmulas de regresión.[1]
A-constant
El A-constant fue diseñado originalmente para la ecuación de SRK y depende de múltiples variables incluyendo IOL fabricante, estilo y colocación dentro del ojo. Debido a su simplicidad, la constante A se convirtió en el valor utilizado para caracterizar los implantes intraoculares.
A-las constantes se utilizan directamente en II SRK y SRK/T fórmulas. La constante es un valor teórico que relaciona la potencia de la lente AL y keratometry, no se expresa en unidades y es específico para el diseño de la lio y la ubicación prevista y orientación dentro del ojo.
Usando A-constantes es práctico cuando una decisión sobre el poder del implante debe hacerse durante la cirugía porque la potencia de la lente varía en una relación 1:1 con la A-constantes: si A disminuye por 1 dioptría, IOL potencia disminuye por 1 dioptría también. Esta relación recta agrega a la simplicidad y la popularidad de la A-constante. Otras constantes que se utilizan en las fórmulas modernas IOL incluyen el valor ACD en fórmulas Binkhorst y Hoffer-Q, el un0, un1y un2 constantes de la fórmula Haigis y el factor cirujano (SF) en fórmulas Holladay. Profundidad verdadera cámara anterior (ACD) se mide entre la superficie corneal posterior y la superficie de la lente anterior. Esta medida no es debe ser confundido con la constante de la cámara anterior (constante de ACD) utilizada en las fórmulas de cálculo de potencia IOL.[2]
Cálculo de la potencia de la lente intraocular después de la cirugía refractiva
Siguiente de la extracción de la catarata cirugía refractiva plantea problemas especiales para el paciente y el cirujano porque el cambio como resultado de la cirugía refractiva corneal complica precisa Queratometría, un elemento clave de la lente del implante cálculo de potencia. Después de cirugía refractiva con láser para la miopía, esto podría resultar en la sobreestimación de la energía córnea, subestimación de la lio potencia requerida y resultados hipermétropes tras cirugía de catarata.
La dificultad surge de varios factores:[1]
- Los instrumentos utilizados por los oftalmólogos para medir el poder corneal (queratómetros, topógrafos corneales) no pueden obtener medidas exactas en los ojos que han sido sometidos a cirugía refractiva de la córnea. La mayoría medida queratómetros manual en la zona de 3 milímetros de la córnea central, que a menudo falta la zona central del aplanador de energía eficaz de la córnea.
- El supuesto índice de refracción de la córnea normal se basa en la relación entre las curvaturas córneas anteriores y posteriores. Esta relación ha cambiado en los ojos LASIK.
- Fórmulas de alimentación IOL mayoría utilizan la longitud axial y keratometric lectura (K) para predecir la posición de la lio postoperatoriamente (ELP). En los ojos post LASIK esto provoca un error en la predicción porque las dimensiones del compartimiento anterior no cambia realmente en estos ojos proporcionalmente con el k mucho más plano. Con el fin de abordar este problema fue desarrollado el método de doble-K, que utiliza el poder corneal pre LASIK para el cálculo del ELP y el poder corneal post LASIK para el cálculo del componente de convergencia de la fórmula.
Véase también
- Lente intraocular
Referencias
- ^ a b c d Curso de ciencia básica y clínica, sección 3: óptica clínica. (2011-2012 ed.). Academia Americana de Oftalmología. págs. 211-223. ISBN978-1615251100.
- ^ a b c Roger F. Steinert, David F. Chang (2010). Cirugía de cataratas (3rd ed. ed.). Saunders. ISBN9781416032250.
- ^ a b c Lee, AC; Qazi, MA; Pepose, JS (enero de 2008). "La biometría y cálculo de la potencia de la lente intraocular. Opinión actual en Oftalmología 19 (1): 13 – 7. Doi:10.1097/ICU.0b013e3282f1c5ad. PMID18090891.
- ^ a b Myron Yanoff, Jay S. Duker (2009). Oftalmología (3rd ed. ed.). Mosby Elsevier. págs. 416-419. ISBN978-0-323-04332-8.
Enlaces externos
Calculadora de la energía de la Lente Intraocular Toric- https://Aurolab.com/auroflextoric-Hydrophilic-IOL.asp Materiales de cálculo de la lente el Dr. Hill- https://www.Doctor-Hill.com/IOL-Main/formulas.htm
Cálculo online de lentes intraoculares usando IOL diferente fórmulas - https://www.Augenklinik.uni-wuerzburg.de/uslab/iolfrme.htm
Otras Páginas
- Presentan valor (seccion una aproximacion para el calculo de la anualidad y prestamo)
- Gordon la taltuza
- Esperanza Fire (categoria montanas del San Jacinto)
- Johns Manville (seccion asbesto litigios y Johns Manville)
- Acuerdo de recompra (seccion vender-comprar lomos y espalda de compra y venta)
- Region norte de Ohio
- Acer X 960
- Escuela Bromfords
- FreeCast (software)