Catenina

Cateninas son una familia de proteínas encontrado en complejos con cadherina adhesión celular moléculas de animal células. Los primeros dos cateninas que se identificaron[2] se conoce como α-catenina y β-catenina. A-catenina puede enlazar a β-catenina y también puede enlazar actinia. B-catenina une el dominio citoplásmico de algunos caderinas. Se han identificado adicionales cateninas γ-catenina y la δ-catenina. El nombre "catenina" fue originalmente seleccionado ('catenaria' significa 'cadena' Latina) porque se sospechaba que cateninas podrían vincular caderinas con el citoesqueleto.[3]
Contenido
- 1 Tipos
- 2 Función
- 2.1 Interacción con caderinas
- 3 Significación clínica
- 3.1 Estudios clínicos recientes
- 3.2 Cateninas en cáncer
- 4 Referencias
- 5 Acoplamientos externos
Tipos
- Α-catenina
- Β-catenina
- Δ-catenina
- Γ-catenina
Todos pero α-catenina contienen repeticiones del armadillo.
Función
Varios tipos de cateninas trabajan con N-caderinas a desempeñar un papel importante el aprendizaje y memoria (Para el artículo completo, vea Complejo cadherina-catenina en el aprendizaje y la memoria).
Adherencia de la célula complejos se requiere simple epitelios en organismos más altos para mantener la estructura, función y polaridad. Estos complejos, que ayudan a regular el crecimiento celular además de crear y mantener las capas epiteliales,[4] se conocen como uniones adherentes y que por lo general incluyen en menos cadherin, β-catenina y α-catenina.[5] Cateninas desempeñan un papel en la organización celular y polaridad mucho antes de que el desarrollo e incorporación de Vías de señalización de Wnt y caderinas.[5][6]
El principal papel mecánico de cateninas conecta cadherins a actinia filamentos, específicamente en las uniones de adhesión de células epiteliales.[7] Mayoría de los estudios investigando acciones catenina centrarse en α-catenina y β-catenina. Β-catenina es particularmente interesante como juega un doble papel en la célula. En primer lugar, atando al receptor Caderina intracelular citoplásmico Dominios de la cola,[8] puede actuar como un componente integral de un complejo en las uniones de la proteína que ayuda a las células mantener capas epiteliales. Β-catenina actúa anclando la actina citoesqueleto las uniones y posiblemente puede ayudar en la inhibición de contacto señalización dentro de la célula.[4][9] Por ejemplo, cuando una capa epitelial es completa y las ensambladuras de los adherens indican que la célula está rodeada, β-catenina puede desempeñar un papel en decirle a la célula para detener la proliferación, como no hay espacio para más células en la zona. En segundo lugar, la β-catenina participa en la vía como destino aguas abajo de señalización de Wnt. Mientras que la vía es muy detallado y no completamente entendido,[10] en general, cuando Wnt no está presente, GSK-3B (un miembro de la vía) es capaz de fosforilan β-catenina como resultado de una formación compleja que incluye β-catenina, AXIN1, AXIN2, APC (un tumor supresor genes producto), CSNK1A1, y GSK3B. Después de fosforilación de la N-terminal Ser y THR residuos de β-catenina, BTRC promueve su ubiquitinación, que provoca que se degrada por el complejo TrCP/SKP.[4][9] Por otro lado, cuando Wnt, GSK-3B es desplazado del mencionado complejo, causando β-catenina para no ser phosphorylated y así no ubiquitinated. Como resultado, se estabilizan sus niveles en la célula como se acumula en el citoplasma. Finalmente, algunos de este β-catenina acumulada se moverán en el núcleo con la ayuda de Rac1.[9] En este punto, la β-catenina se convierte un coactivator para TVC y LEF desplazando a Groucho y HDAC represores de transcripción para activar genes Wnt.[4][9] Estos productos génicos son importantes en la determinación de destinos celulares durante el desarrollo normal y en el mantenimiento de la homeostasis,[11] o pueden llevar al crecimiento de regulado en trastornos como el cáncer por responder a las mutaciones de la β-catenina, APC o Axin, cada uno de ellos puede conducir a esta estabilización nivel regulado de β-catenina en las células.[9]
Mientras menos atención se dirige a α-catenina en estudios realizados en la adhesión celular, sin embargo, es un jugador importante en el crecimiento, función y organización celular. Α-catenina participa en la formación y estabilización de las uniones por Unión a complejos cadherina-catenina-β en la célula.[8] Los mecanismos exactos por los cuales α-catenina actúa en las uniones es todavía confusa; sin embargo, es probable que α-catenina actúa en concierto con vinculin se unen a actina y ayudar a estabilizar a las uniones.[8]
Interacción con caderinas
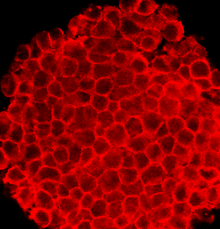
Células de carcinoma embrionario F9 son similares a los Células P19 se muestra en la figura 1 y normalmente ha adhesión de célula a célula mediada por E-cadherina con β-catenina al dominio citoplásmico de la E-cadherina. Las células F9 fueron genéticamente modificadas para carecer de β-catenina, lo que resulta en la mayor asociación de plakoglobin con E-cadherina.[12] En las células F9 que carecen de β-catenina y plakoglobin, muy poco E-cadherina y α-catenina acumulan en la superficie celular.[12] Ratones que carecen de β-catenina tienen embriones defectuosos. Ratones diseñados para específicamente vascular endotelio las células deficientes en β-catenina mostraron problemas de adherencia entre las células endoteliales vasculares.[13] Ratones que carecen de plakoglobin tienen defectos de adhesión celular en muchos tejidos, aunque sustituye a β-catenina por plakoglobin en muchas uniones celulares.[14] Queratinocitos para no expresar alfa-catenina han interrumpido la adhesión celular[15] y activado NF-ΚB.[16] Un tumor de células con defecto δ-catenina, bajos niveles de E-cadherina y pobre adherencia a la célula podía ser restaurada a la morfología epitelial normal y aumento de los niveles de E-cadherina expresión de niveles normales de δ-catenina funcional.[15]
Significación clínica
Como se mencionó anteriormente, las mismas propiedades de catenina que le da un papel importante en la determinación de destino normal de la célula, la homeostasis y el crecimiento, también lo hacen susceptible a las alteraciones que pueden conducir a crecimiento y comportamiento celular anormal. Cualquier cambio en la organización del citoesqueleto y de la adherencia puede conducir a señalización alterada, migración y pérdida de inhibición de contacto puede promover la formación del desarrollo y del tumor del cáncer.[17][18] En particular, se han identificado cateninas a ser actores principales en el crecimiento de la capa de célula epitelial aberrante asociada a varios tipos de cáncer. Mutaciones en genes que codifican estas proteínas pueden llevar a la inactivación de las adherencias de cadherina de la célula y la eliminación de la inhibición de contacto, permitiendo que las células a proliferar y migrar, promoviendo desarrollo tumorigenesis y cáncer.[7] Cateninas son conocidos por estar asociados con colorrectal y cáncer de ovario, y se han identificado en pilomatrixoma, meduloblastoma, adenomas pleomórficosy malos mesotelioma.[4]
Mientras menos se conoce el mecanismo exacto de la α-catenina, su presencia en cáncer se siente ampliamente. A través de la interacción de β-catenina, actina y α-catenina y E-cadherin están vinculados, la célula proporciona un medio de adhesión celular estable. Sin embargo, disminuye en esta capacidad de adherencia de la célula se ha relacionado con la progresión de la metástasis y del tumor.[19] En las células normales, α-catenina puede actuar como un supresor de tumor y puede ayudar a prevenir los defectos de adherencia asociados con el cáncer. Por otro lado, la falta de α-catenina puede promover la transcripción aberrante, que puede conducir a cáncer.[17][20][21] Como resultado, se puede concluir,[17][20][22] cánceres que más a menudo posible asociados con disminución de los niveles de α-catenina.
Β-catenina también es probable que juega un papel importante en diversas formas de desarrollo de cáncer. Sin embargo, a diferencia de la α-catenina, niveles de aumento de β-catenina pueden ser asociados con la carcinogénesis. En particular, las interacciones anormales entre las células epiteliales y la matriz extracelular están asociadas con la sobreexpresión de estos β-cateninas y su relación con caderinas en algunos tipos de cáncer.[22][23][24] Estimulación de la vía Wnt/β-catenina y su papel en la promoción de formaciones de tumor malignos y metástasis, también se ha implicado en casos de cáncer.[25]
El papel de catenina en transición epitelial-mesenquimal (o EMT) también ha recibido mucha atención recientemente por sus contribuciones al desarrollo de cáncer. Se ha demostrado HIF-1Α puede inducir la vía de la EMT, así como Vía de señalización Wnt/β-catenina, aumentando así el potencial invasor de las células LNCaP (células humanas de cáncer de próstata).[26] Como resultado, es posible que la EMT asociada a upregulated que HIF-1α es controlado por señales de este camino de Wnt/β-catenina.[26] Las interacciones catenina y EMT también pueden desempeñar un papel en el carcinoma hepatocelular. VEGF-B tratamiento de las células del hepatoma carcinoma puede causar α-catenina mover de su ubicación normal en la membrana en el núcleo y la expresión de cadherina-para disminuir, promoviendo así la invasión de EMT y del tumor.[27]
Hay otros factores fisiológicos que se asocian con el desarrollo de cáncer a través de sus interacciones con las cateninas. Por ejemplo, mayores niveles de colágeno XXIII se han asociado con niveles más altos de cateninas en las células. Estos niveles elevados de colágeno ayudó a facilitar las adherencias y crecimiento independiente de anclaje celular y proporcionaron la evidencia del papel de colágeno XXIII en la mediación metástasis.[28] En otro ejemplo, la señalización de Wnt/β-catenina ha sido identificado como activar microARN-181s en carcinoma hepatocelular que juegan un papel en la tumorigénesis.[29]
Estudios clínicos recientes
Recientemente, ha habido un número de estudios en el laboratorio y en la clínica investigando nuevas posibles terapias para cánceres asociados con catenina. Antagonistas de la integrina y immonochemotherapy con 5-fluorouracilo más polisacárido-K han mostrado resultados prometedores.[22] Polisacárido K puede promover apoptosis inhibiendo NF-ΚB activación, que es normalmente para arriba-regulados e inhibiendo apoptosis, cuando se aumentan los niveles de β-catenina en cáncer. Por lo tanto, polisacárido K para inhibir la activación de NF-κB puede se usar para tratar a pacientes con niveles altos de β-catenina.[30]
En el tratamiento actual a corto plazo, para combinar técnicas con terapias dirigidas a elementos asociados catenina de cáncer podrían ser más eficaces en el tratamiento de la enfermedad. Interrumpiendo la Wnt/β-catenina señalización vías, radioterapia neoadyuvante a corto plazo (STNR) puede ayudar a prevenir la recurrencia clínica de la enfermedad después de la cirugía, pero se necesita mucho más trabajo antes de un tratamiento adecuado basado en este concepto se puede determinar.[31]
Estudios de laboratorio también han implicado potenciales dianas terapéuticas para futuros estudios clínicos. VEGFR-1 y EMT mediadores pueden ser blancos ideal para prevenir el desarrollo de cáncer y metástasis.[27] 5-aminosalicilato (ASA) ha demostrado reducir la β-catenina y su localización en el núcleo en las células de cáncer de colon aisladas y en pacientes. Como resultado, puede ser útil como un agente chemopreventative para el cáncer colorrectal.[32] Además, acil aldehidos han demostrado inhibir la Wnt de señalización característica de muchos tipos de cáncer por desestabilizar la β-catenina, interrumpiendo así Wnt de señalización y prevención del crecimiento de células aberrantes asociados con el cáncer.[33] Por otra parte, algunos conceptos de tratamiento implican regular el sistema de adhesión E-cadherina/catenina para evitar interrupciones en las adherencias y la inhibición de contacto de la promoción de metástasis del cáncer. Una forma posible de lograrlo, que ha tenido éxito en modelos de ratón, es utilizar inhibidores de la activación de Ras con el fin de mejorar la funcionalidad de estos sistemas de adherencia.[34] Otra catenina, cadherina o reguladores de ciclo celular también pueden ser útiles en el tratamiento de una variedad de cánceres.[31][35][36]
Mientras que estudios recientes en el laboratorio y en la clínica han dado resultados prometedores para el tratamiento de varios tipos de cáncer asociados catenina, la vía Wnt/β-catenina puede hacer difícil a un solo objetivo terapéutico correcto como se ha mostrado el camino para obtener una variedad de diferentes acciones y funciones, algunas de las cuales posiblemente incluso podría para ser anti oncogénica.[25]
Cateninas en cáncer
Resumen:
- Cánceres asociados: colorrectal y cáncer de ovario; pilomatrixoma; meduloblastoma; adenomas pleomórficos; malo mesotelioma; glioblastomas.[4][37]
- Mutaciones en genes de catenina pueden causar pérdida de inhibición de contacto puede promover la formación del desarrollo y del tumor del cáncer.[17][18]
- Mutaciones asociadas con crecimiento de la capa de célula epitelial aberrante debido a la falta de adherencias y la inhibición de contacto
- Regula los niveles de α-catenina
- Para arriba-regula los niveles de β-catenina
- Estimulación de la vía Wnt/β-catenina
- Catenina alteración (y camino de Wnt/β-catenina para arriba-regulación) pueden ayudar a estimular transición epitelial-mesenquimal (o EMT)
- Las mutaciones o la regulación aberrante de cateninas también puede asociarse otros factores que promueven la metástasis y tumorogénesis
- Tratamientos se concentran en corregir niveles de catenina aberrante o regular vías de catenina que están asociadas con el desarrollo del cáncer y la progresión
Referencias
- ^ Weis WI, Nelson WJ (noviembre de 2006). «Volver a resolver el Acertijo de la cadherina-catenina-actina». J Biol Chem. 281 (47): 35593-7. doi:10.1074/jbc. R600027200. PMC3368706. PMID17005550.
- ^ Peyriéras N, D Louvard, Jacob F (diciembre de 1985). "Caracterización de los antígenos reconocidos por anticuerpos monoclonales y policlonales dirigidos contra uvomorulin". Estados Unidos el proc. nacional Acad. SCI. 82 (23): 8067 – 71. doi:10.1073/pnas.82.23.8067. PMC391443. PMID2415979.
- ^ Ozawa M, Baribault H, Kemler R (junio de 1989). "El dominio citoplásmico de la uvomorulin de molécula de adhesión celular se asocia con tres independientes proteínas estructuralmente relacionadas en diferentes especies". EMBO J. 8 (6): 1711-7. PMC401013. PMID2788574.
- ^ a b c d e f "Β-catenina". Sino biológico Inc.: Especialista en solución biológica.
- ^ a b Reynolds AB (junio de 2011). "Organización epitelial: nueva perspectiva en la α-catenina de una fuente antigua". Curr. Biol 21 (11): R430-2. doi:10.1016/j.Cub.2011.04.043. PMID21640901.
- ^ Dickinson DJ, Nelson WJ, Weis WI (marzo de 2011). "un epitelio polarizado organizado por β - y α-catenina es anterior a Caderina y metazoarios orígenes". Ciencia 331 (6022): 1336 – 9. doi:10.1126/Science.1199633. PMC3152298. PMID21393547.
- ^ a b Hirohashi S, Kanai Y (julio de 2003). sistema de adhesión celular y morfogénesis cáncer en humanos. Cáncer SCI. 94 (7): 575-81. doi:10.1111/j.1349-7006.2003.tb01485.x. PMID12841864.
- ^ a b c Rangarajan ES, Izard T (abril de 2012). "Α-catenina despliega en Unión a vinculin." J Biol Chem 287 (22): 18492-9. doi:10.1074/jbc. M112.351023. PMID22493458.
- ^ a b c d e "Señalización de Wnt/β-catenina". Tecnología de señalización de la célula. De noviembre de 2010.
- ^ Mosimann C, Hausmann G, Basler K (abril de 2009). "β-catenina hits cromatina: regulación de la activación de Wnt objetivo gene". Biología Molecular de la célula de naturaleza comentarios 10 (4): 276 – 86. doi:10.1038/nrm2654. PMID19305417.
- ^ MacDonald BT, Tamai K, que X (julio de 2009). "señalización de Wnt/β-catenina: componentes, mecanismos y enfermedades". Célula de dev. 17 (1): 9 – 26. doi:10.1016/j.devcel.2009.06.016. PMC2861485. PMID19619488.
- ^ a b Fukunaga Y, Liu H, Shimizu M, Komiya S, Kawasuji M, Nagafuchi A (2005). «Definición de los papeles de β-catenina y plakoglobin en la adhesión célula-célula: aislamiento de las células F9 de β-catenina plakoglobin-deficientes ". Estructura de la célula. FUNCT. 30 (2): 25 – 34. doi:10.1247/CSF.30.25. PMID16357441.
- ^ Cattelino A Liebner S R Gallini, Zanetti A, Balconi G, Corsi A, Bianco P, H Wolburg, Moore R, Oreda B, R de Kemler, Dejana E (septiembre de 2003). "la inactivación condicional del gen β-catenina en las células endoteliales provoca un patrón vascular defectuosa y una mayor fragilidad vascular". J. Biol de la célula 162 (6): 1111 – 22. doi:10.1083/JCB.200212157. PMC2172846. PMID12975353.
- ^ Bierkamp C, H Schwarz, Huber O, R de Kemler (enero de 1999). "Desmosomal localización de β-catenina en la piel de los ratones mutantes nulos de plakoglobin". Desarrollo 126 (2): 371-81. PMID9847250.
- ^ a b Vasioukhin V, Bauer C, Degenstein L, sabio B, Fuchs E (febrero de 2001). hiperproliferación y defectos en la polaridad epitelial sobre ablación condicional de alfa-catenina en la piel. Célula 104 (4): 605 – 17. doi:10.1016/S0092-8674 (01) 00246-X. PMID11239416.
- ^ Kobielak A, Fuchs E (febrero de 2006). "Vínculos entre alfa-catenina, NF-kappaB y de células escamosas en la piel". Estados Unidos el proc. nacional Acad. SCI. 103 (7): 2322 – 7. doi:10.1073/pnas.0510422103. PMC1413714. PMID16452166.
- ^ a b c d V Tripathi, Popescu NC, Zimonjic DB (abril de 2012). DLC1 interacción con α-catenina estabiliza a las uniones y mejora actividad antioncogenic DLC1. Mol Cell Biol 32 (11): 2145 – 59. doi:10.1128/MCB.06580-11. PMID22473989.
- ^ a b Buda A, Pignatelli M (diciembre de 2011). E-cadherina y la red citoesquelética en el desarrollo de cáncer colorrectal y metástasis. Común de la célula. Adhes. 18 (6): 133-43. doi:10.3109/15419061.2011.636465. PMID22176698.
- ^ Tanaka T, M Iino, Goto K (marzo de 2012). "Caída de Sec6 mejora la adherencia de la célula incrementando E-α-catenina en células de cáncer oral". FEBS Lett. 586 (6): 924 – 33. doi:10.1016/j.febslet.2012.02.026. PMID22381337.
- ^ a b Flores ER, Halder G (2011). "la proliferación de células en la piel: alfa-catenina se lleva sobre el camino de hipopótamo". Señal de SCI 4 (183): pe34. doi:10.1126/scisignal.2002311. PMID21791701.
- ^ Silvis Señor Kreger BT, Lien WH, O Klezovitch, Rudakova GM, Camargo FD, Lantz DM, JT Seykora, Vasioukhin V (2011). «Α-catenina es un supresor de tumores que controla la acumulación celular mediante la regulación de la localización y actividad del transcripcional del coactivator Yap1». Señal de SCI 4 (174): ra33. doi:10.1126/scisignal.2001823. PMC3366274. PMID21610251.
- ^ a b c Drivalos A, Papatsoris AG, Chrisofos M, E Efstathiou, Dimopoulos MA (2011). "El papel de las moléculas de adhesión celular (integrinas/caderinas) en cáncer de próstata". Int Braz J Urol 37 (3): 302 – 6. doi:10.1590/S1677-55382011000300002. PMID21756376.
- ^ F de Zhang, Meng F, Li H, Y Dong, Yang W, Han una (septiembre de 2011). "Supresión de retinoid X receptor alfa y expresión aberrante de β-catenina significativamente asociados con la progresión del carcinoma colorrectal". Cáncer de EUR J. 47 (13): 2060-7. doi:10.1016/j.ejca.2011.04.010. PMID21561764.
- ^ Stauffer JK, Scarzello AJ, Andersen JB, De Kluyvera RL, nuevo TC, JM Weiss, Thorgeirsson SS, Wiltrout RH (abril de 2011). "Coactivation de AKT y β-catenina en ratones rápidamente induce la formación de tumores lipogénicos hígado". Cáncer Res. 71 (7): 2718-27. doi:10.1158/0008-5472.CAN-10-2705. PMC3074499. PMID21324921.
- ^ a b Guardavaccaro D: Clevers H (2012). "Wnt/β-catenina y señalización MAPK: aliados y enemigos en diferentes campos de batalla". Señal de SCI 5 (219): pe15. doi:10.1126/scisignal.2002921. PMID22494969.
- ^ a b Zhao JH, Y Luo, Jiang YG, lo DL, Wu CT (julio de 2011). "Precipitación de β-catenina a shRNA causa una reversión de la EMT y fenotipos metastásicos inducidas por HIF-1α". Cáncer Invest. 29 (6): 377 – 82. doi:10.3109/07357907.2010.512595. PMID21649463.
- ^ a b Feng LJ, Xiang Z, ZY Yi, Yao H (2011). "activación del receptor 1 de factor de crecimiento endotelial vascular media transición de epitelio a mesénquima de las células del carcinoma hepatocelular". J Invest Surg 24 (2): 67 – 76. doi:10.3109/08941939.2010.542272. PMID21345006.
- ^ Spivey KA, Chung I, J Banyard, forma I, Feldman HA, Zetter BR (octubre de 2011). "Un papel de colágeno XXIII en metástasis, independencia de anclaje y adherencia de la célula de cáncer". Oncogén 31 (18): 2362-72. doi:10.1038/ONC.2011.406. PMID21963851.
- ^ Ji J, Yamashita T, Wang XW (2011). "señalización de Wnt/β-catenina activa expresión de microRNA-181 en hepatocarcinoma". Celular Biosci 1 (1): 4. doi:10.1186/2045-3701-1-4. PMC3116242. PMID21711587.
- ^ Yamashita K, Ougolkov AV, Nakazato H, Ito K, Ohashi Y, H de Ishinomaki, Yasumoto K, Omote K, AMI M, Takahashi Y, Minamoto T (agosto de 2007). "Immunochemotherapy ayudante con polisacárido K de la protein-bound para cáncer de colon en relación con la activación oncogénica de β-catenina". Esquema de Colon recto 50 (8): 1169 – 81. doi:10.1007/s10350-006-0842-5. PMID17347903.
- ^ a b N Gassler, Herr I, Keith M, F Autschbach, Schmitz Winnenthal H, Ulrich A, Otto HF, Kartenbeck J, Z'graggen K (diciembre de 2004). Señalización Wnt y apoptosis después de la radioterapia a corto plazo neoadyuvante para el cáncer rectal. Int j Oncol. 25 (6): 1543 – 9. doi:10.3892/Ijo.25.6.1543. PMID15547689.
- ^ J Munding, W Ziebarth, Pox CP, Ladigan S, Reiser M, Hüppe D, marca L, Schmiegel W, Tannapfel A, CA Reinacher Schick (marzo de 2012). "La influencia del ácido 5-aminosalicílico en la progresión de los adenomas colorrectales mediante la vía de señalización de β-catenina". Carcinogénesis 33 (3): 637 – 43. doi:10.1093/carcin/bgr306. PMID22198215.
- ^ Canción S, Christova T, Perusini S, Alizadeh S, Bao RY, Miller BW, Hurren R, Jitkova Y, M Gronda, Isaac M, José B, Subramaniam R, Aman A, Chau A, DE Hogge, vertedero SJ, Kasper J, Schimmer AD, R Al-awar, Wrana JL, Attisano L (diciembre de 2011). "Wnt inhibidor pantalla muestra dependencia de hierro de β-catenina en cáncer". Cáncer Res. 71 (24): 7628, 39. doi:10.1158/0008-5472.CAN-11-2745. PMID22009536.
- ^ Nam JS, Ino Y, Sakamoto M, Hirohashi S (septiembre de 2002). Ras farnesylation inhibidor FTI-277 restaura el sistema de adherencia de célula de E-cadherina/catenina en células cancerosas humanas y reduce la metástasis del cáncer. JPN. J. cáncer Res. 93 (9): 1020 – 8. doi:10.1111/j.1349-7006.2002.tb02479.x. PMID12359056.
- ^ Singh M, Darcy KM, Brady nos, Clubwala R, Weber Z, Rittenbach JV, Akalin A, Whitney CW, Zaino R, Ramirez NC, Leslie KK (noviembre de 2011). "caderinas, cateninas y ciclo celular reguladores: impacto sobre la supervivencia en una fase de grupo oncológico ginecológico cáncer endometrial II ensayo". PCO.OOI Oncol. 123 (2): 320-8. doi:10.1016/j.ygyno.2011.07.005. PMC3518446. PMID21813170.
- ^ F Coluzzi, Mandatori I, Mattia C (septiembre de 2011). "Terapias emergentes en el dolor óseo metastásico". Expertos Opin Emerg drogas 16 (3): 441 – 58. doi:10.1517/14728214.2011.576668. PMID21545247.
- ^ Yang, C; Iyer, RR; Yu, CA; Yong, RL; Parque, DM; Weil, RJ; Ikejiri, B; Brady, RO; Lonser, RR; Zhuang, Z (mayo de 2012). señalización de β-catenina inicia la activación de astrocitos y su disregulación contribuye a la patogenesia de los astrocitomas. Proc Natl Acad Sci U S A 109 (18): 6963 – 8. doi:10.1073/pnas.1118754109. PMID22505738.
Acoplamientos externos
- Cateninas en la Biblioteca Nacional de Estados Unidos de la medicina Encabezamientos de temas médicos (MeSH)
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||