Granulomatosis con poliangeítis
| Granulomatosis de Wegener con poliangeítis | |
|---|---|
| Clasificación y recursos externos | |

Micrografía presentan elementos característicos de la granulomatosis de Wegener - un vasculitis y granulomas con las células gigantes multi nucleadas. Tinción H & E.
|
|
| CIE-10 | M31.3 |
| CIE-9 | 446.4 |
| DiseasesDB | 14057 |
| MedlinePlus | 000135 |
| eMedicine | Med/2401 |
| Paciente UK | Granulomatosis con poliangeítis |
| Malla | D014890 |
Granulomatosis con poliangeítis Conocido (GPA), anteriormente como Granulomatosis de Wegener (WG), es un desorden sistémico que implica tanto Granulomatosis y polyangiitis. Es una forma de vasculitis (inflamación de los vasos sanguíneos) que afecta a los vasos pequeños y medianos en muchos órganos. Daño a la pulmones y riñones puede ser fatal. Se requiere a largo plazo inmunosupresión.[1] Cuando se refirió a como granulomatosis de Wegener, es el nombre de Friedrich Wegener, que describe la enfermedad en 1936.[2] Debido a la Asociación de Wegener con el Partido Nazi alemán, cuerpos profesionales y revistas han sustituido su nombre con un nombre descriptivo.[3]
Granulomatosis con polyangiitis es parte de un grupo de síndromes vasculitic llamado vasculitides sistémicos o vasculopathies, todos los cuales cuentan con un ataque autoinmune por un tipo anormal de circulante de necrotización anticuerpo denominado ANCAs (anticuerpos citoplasmáticos Antineutrófilo) contra pequeñas y de tamaño mediano vasos sanguíneos. Aparte de GPA, esta categoría incluye Síndrome de Churg-Strauss y polyangiitis microscópico.[1] Aunque GPA afecta vasos de tamaño pequeño y mediano,[4] formalmente se clasifica como uno de los vasos vasculitides en el sistema de Chapel Hill.[5]
Contenido
- 1 Signos y síntomas
- 2 Causas
- 3 Fisiopatología
- 4 Diagnóstico
- 4.1 Criterios
- 5 Tratamiento
- 6 Pronóstico
- 7 Epidemiología
- 8 Historia
- 9 Referencias
- 10 Enlaces externos
Signos y síntomas
Signos iniciales son extremadamente variables, y diagnóstico puede retrasarse severamente debido a la naturaleza no específica de la síntomas. En general, rinitis es la primera señal en la mayoría de la gente.[1][6]
- Riñón: Glomerulonefritis rápidamente progresiva (75%), llevando a insuficiencia renal crónica
- Vías respiratorias superiores, ojo y oreja enfermedad:
- Nariz: dolor, congestión, hemorragias nasales, rinitis, formación de costras, silla de montar-nariz deformidad debido a un tabique perforado
- Orejas: conductora pérdida de la audición debido a tubo auditivo disfunción, hipoacusia neurosensorial (mecanismo claro)
- Cavidad bucal: gingivitis fresa, subyacente a la destrucción del hueso con el aflojamiento de los dientes, inespecífica ulceraciones en la mucosa oral
- Ojos: seudotumores, Escleritis, conjuntivitis, uveítis, Episcleritis
- Tráquea:: subglótico estenosis
- Pulmones:: nódulos pulmonares (denominados "lesiones de moneda"), infiltrados (a menudo interpretados como neumonía), lesiones cavitarias, hemorragia pulmonar causando hemoptisisy estenosis bronquial raramente.
- Artritis:: Dolor o hinchazón (60%), a menudo inicialmente diagnosticados como artritis reumatoide
- Piel:: nódulos en el codo, púrpura, varios otros (véase vasculitis cutánea)
- Sistema nervioso:: ocasionalmente neuropatía sensorial (10%) y raramente mononeuritis múltiple
- Corazón, tracto gastrointestinal, cerebro, otros órganos: raramente afectados.
Causas
Sus causas son desconocidas, aunque los microbios, como bacterias y virus, así como genética han sido implicados en su patogénesis.[6][7]
Fisiopatología
Inflamación con granuloma formación contra un fondo inflamatorio no específico es la anormalidad clásico tejido en todos los órganos afectados por GPA.[1]
Ahora se presume ampliamente que el anticuerpos citoplásmicos del anti-neutrófilo (ANCAs) son responsables de la inflamación en promedio.[1] Los típicos ANCAs en promedio son aquellos que reaccionan con proteinasa 3, una enzima prevalente en granulocitos neutrófilos.[8]
In vitro los estudios han encontrado que pueden activar ANCAs neutrófilos, aumentar su adhesión a endotelioe induce su degranulación que puede dañar células endoteliales. En teoría, este fenómeno podría causar grandes daños en la pared del vaso, en particular de arteriolas.[1]
Diagnóstico
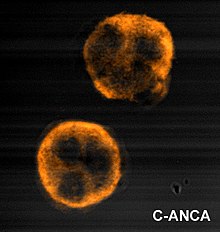

Granulomatosis con polyangiitis generalmente se sospecha sólo cuando una persona ha tenido inexplicables síntomas durante un largo periodo de tiempo. Determinación de la Anticuerpos citoplásmicos del anti-neutrófilo (ANCAs) puede ayudar en el diagnóstico, pero la positividad no es concluyente y ANCAs negativos no son suficientes para rechazar el diagnóstico. ANCAs de coloración citoplásmicos que reaccionan con la enzima proteinasa 3 (cANCA) en neutrófilos (un tipo de glóbulos blancos) se asocian con GPA.[1]
Si la persona tiene insuficiencia renal o vasculitis cutánea, un biopsia se obtiene de los riñones. En raras ocasiones, toracoscópica la biopsia del pulmón se requiere. En histopatológica el examen, mostrará una biopsia vasculitis leucocitoclástica con necrótico cambios y granulomatosa inflamación (agrupaciones de glóbulos blancos normalmente dispuestos) en Microscopía. Estos granulomas son la principal razón de la denominación de "Granulomatosis de Wegener", aunque no es una característica esencial. Sin embargo, los granulomas necrotizante son un rasgo distintivo de esta enfermedad. Sin embargo, muchas biopsias pueden ser inespecíficas y 50% proporcionan muy poca información para el diagnóstico de GPA.[1]
Criterios
En 1990, la Colegio estadounidense de Reumatología Criterios de clasificación aceptada de GPA. Estos criterios no fueron pensados para el diagnóstico, pero para su inclusión en ensayos controlados aleatorios. Dos o más criterios positivos tienen una sensibilidad del 88,2% y una especificidad del 92.0% de describir el GPA.[9]
- Inflamación nasal u oral:
- úlceras orales dolorosas o indoloras or
- purulenta o secreción nasal sangriento
- Pulmones: radiografía de tórax anormal con:
- nódulos,
- infiltra or
- cavidades
- Riñones: sedimento urinario con:
- microhematuria or
- glóbulo rojo moldes
- Biopsia: la inflamación granulomatosa
- dentro de la pared arterial or
- en el área perivascular
Según el Conferencia de consenso de Chapel Hill (CHCC) en la nomenclatura de las vasculitis sistémicas (1992), establecer el diagnóstico de GPA demandas:[10]
- a granulomatosa inflamación del tracto respiratorio, y
- a vasculitis de pequeñas a medianas embarcaciones.
Varios investigadores han comparado los criterios ACR y Chapel Hill.[11]
Tratamiento
Es el tratamiento estándar para GPA ciclofosfamida y dosis altas corticoesteroides para la inducción de la remisión y menos tóxicas como inmunosupresores azatioprina, leflunomida, metotrexato o micofenolato mofetil.[12] Trimetoprima/sulfametoxazol también puede ayudar a prevenir la recaída.[12] Rituximab puede ser sustituido por ciclofosfamida en la inducción de la remisión.[12][13] A revisión sistemática de 84 ensayos analizó las pruebas para varios tratamientos en promedio. Muchos ensayos incluyen datos sobre los grupos de personas con GPA y polyangiitis microscópico. En esta revisión, los casos se dividen entre enfermedad localizada, no-órgano amenazando, enfermedad mortal órgano generalizada y la vasculitis renal severa y enfermedad inmediatamente peligrosa para la vida.[14]
- En la enfermedad generalizada no órgano-amenazante, la remisión puede ser inducida con metotrexato y esteroides, donde se reduce la dosis de esteroides después de que se ha logrado una remisión y metotrexato utilizado como mantenimiento.
- En caso de enfermedad mortal órgano, pulsada intravenoso se recomienda la ciclofosfamida con esteroides. Una vez alcanzada la remisión, azatioprina y los esteroides pueden utilizarse para mantener la remisión.
- En vasculitis renal severa, se utiliza el mismo régimen, pero con la adición de plasmaféresis.
- En hemorragia pulmonar, altas dosis de ciclofosfamida con pulsos metilprednisolona puede ser utilizado, o alternativamente CYC, esteroides y el recambio plasmático.
Pronóstico
Hoy en día, con los corticoesteroides y ciclofosfamida, supervivencia a 5 años es superior al 80%.[6] Las complicaciones a largo plazo son comunes (86%), principalmente insuficiencia renal crónica, pérdida de la audición y sordera.[1]
Antes de tratamientos modernos, la mortalidad de 2 años fue más 90% y el promedio de supervivencia de cinco meses.[6][15] La muerte generalmente se producían por uremia o insuficiencia respiratoria.[6]
Epidemiología
El incidencia es de 10 a 20 casos por millón por año.[14][16] Es extremadamente raro en Japón y Afroamericanos.[16]
Historia
Escocés otorrinolaringólogo Peter McBride (1854 – 1946) describió la condición por primera vez en 1897 en un BMJ artículo titulado "Las fotografías de un caso de la destrucción rápida de la nariz y la cara".[17] Heinz Karl Ernst Klinger (nacido en 1907) añadir información sobre la anatomía patológica, pero el cuadro completo fue presentado por Friedrich Wegener (1907-1990), un Alemán patólogo, en dos informes en 1936 y 1939.[2]
Era un nombre anterior de la enfermedad granulomatosis de pathergic.[18] La enfermedad es todavía a veces confundida con granuloma letal de la línea media y granulomatosis linfomatoide, ambos maligno linfomas.[19]
En 2006, Alexander Woywodt)PrestonReino Unido) y Eric Matteson (Mayo ClinicEstados Unidos) investigan el pasado de la granulomatosis de Wegener y descubrió que era, al menos en algún momento de su carrera, un seguidor del régimen Nazi. Además, los datos indican que Wegener era buscado por las autoridades polacas y que sus expedientes fueron transmitidos a la Comisión de crímenes de guerra de las Naciones Unidas. Además, Wegener trabajó en proximidad cercana a la maquinaria de genocidio en Łódź. Sus datos levanten serias dudas sobre la conducta profesional de la granulomatosis de Wegener. Sugieren que el epónimo abandonarse y proponer "vasculitis granulomatosa asociada a ANCA."[20] Los autores que han hecho campaña para que otros epónimos médicos ser abandonada, también.[21] En 2011, la Colegio estadounidense de Reumatología (ACR), la American Society of Nephrology (ASN) y el Liga Europea contra el reumatismo (EULAR) decidió cambiar el nombre a granulomatosis con polyangiitis.[3]
Referencias
- ^ a b c d e f g h i SEO P, piedra JH (julio de 2004). "El Antineutrófilo citoplasmáticos anticuerpo-asociada vasculitides". Soy J. Med. 117 (1): 39-50. Doi:10.1016/j.amjmed.2004.02.030. PMID15210387.
- ^ a b synd/2823 en ¿Quién lo nombró?
- ^ a b Falk RJ, WL bruto, Guillevin L et al (2011). "Granulomatosis con polyangiitis (granulomatosis de Wegener): un nombre alternativo para la granulomatosis de Wegener". Ann Rheum. Dis. 70:: 74. Doi:10.1136/ARD.2011.150714. PMID21372195.
- ^ Gota, CE (mayo de 2013). "Granulomatosis con Polyangiitis (GPA): Vasculitis". Merck Manual Professional. Merck Sharp & Dohme Corp. 16 de marzo de 2014.
- ^ Silva, Fred; Jennette, Charles J.; Más, Robert H.; Olson, Jean T.; Schwartz, Melvin (2007). Patología del Hepinstall del riñón. Hagerstwon, MD: Lippincott Williams & Wilkins. p. 677. ISBN0-7817-4750-3.
- ^ a b c d e Berden, A; Göçeroglu, A; Jayne, D; Luqmani, R; Rasmussen, N; Bruijn, JA; Bajema, (enero 2012). "Diagnóstico y tratamiento de ANCA vasculitis asociaron.". BMJ 344:: e26. Doi:10.1136/bmj.E26. PMID22250224.
- ^ Tracy, CL; Papadopoulos, PJ; Adiós, señor; Connolly, H; Goldberg, E; O ' Brian, RJ; Sharma, GD; Talavera, F; Toder, DS; Valentini, RP; Windle, ML; Lobo, RE (10 de febrero de 2014). "Granulomatosis con Polyangiitis". En el diamante, HS. Medscape Reference. WebMD. 16 de marzo de 2014.
- ^ van der Woude FJ, Rasmussen N, Lobatto S, et al (febrero de 1985). "Los autoanticuerpos contra neutrófilos y monocitos: herramienta para el diagnóstico y marcador de actividad de la enfermedad en granulomatosis de Wegener". The Lancet 1 (8426): 425 – 9. Doi:10.1016/S0140-6736 (85) 91147-X. PMID2857806.
- ^ Leavitt RY, Fauci AS, Bloch DA, et al (agosto de 1990). "The American College of Rheumatology 1990 criterios para la clasificación de la granulomatosis de Wegener". Artritis Rheum. 33 (8): 1101 – 7. Doi:10.1002/Art.1780330807. PMID2202308.
- ^ Jennette JC, Falk RJ, Andrassy K, et al (febrero de 1994). "Nomenclatura de vasculitides sistémicos. Propuesta de una conferencia de consenso internacional". Artritis Rheum. 37 (2): 187 – 92. Doi:10.1002/Art.1780370206. PMID8129773.
- ^ Bruce, en campana AL (abril de 1997). "Una comparación de dos sistemas de nomenclatura para vasculitis sistémica primaria". Br. J. Rheumatol. 36 (4): 453-8. Doi:10.1093/Rheumatology/36.4.453. PMID9159539.
- ^ a b c Tracy, CL; Papadopoulos, PJ; Adiós, señor; Connolly, H; Goldberg, E; O ' Brian, RJ; Sharma, GD; Talavera, F; Toder, DS; Valentini, RP; Windle, ML; Lobo, RE (10 de febrero de 2014). "Granulomatosis con Polyangiitis tratamiento & Management". En el diamante, HS. Medscape Reference. WebMD. 16 de marzo de 2014.
- ^ Tarabishy, AB; Schulte, M; Bent, GN; Hoffman, GS (septiembre – octubre 2010). "Granulomatosis de Wegener: manifestaciones clínicas, diagnóstico diferencial y manejo de enfermedades oculares y sistémicas.". Encuesta de Oftalmología. 55 (5): 429 – 44. Doi:10.1016/j.survophthal.2009.12.003. PMID20638092.
- ^ a b Bosch X, Guilabert A, Espinosa G, Mirapeix E (2007). "Tratamiento de anticuerpos citoplasmáticos Antineutrófilo vasculitis asociada: una revisión sistemática". JAMA 298 (6): 655 – 69. Doi:10.1001/Jama.298.6.655. PMID17684188.
- ^ Smith, RM; Jones, RB; Jayne, DR (abril de 2012). "Progreso en el tratamiento de la vasculitis ANCA-asociados". (PDF). Terapia y la investigación sobre la artritis 14 (2): 210. Doi:10.1186/ar3797. PMC3446448. PMID22569190.
- ^ a b Cartin-Ceba, R; Peikert, T; Manchas, U (diciembre de 2012). "Patogenesia de vasculitis ANCA-asociados". Informes actuales de Reumatología 14 (6): 481 – 93. Doi:10.1007/s11926-012-0286-y. PMID22927039.
- ^ Friedmann me (1982). McBride y el síndrome de granuloma midfacial. (El segundo ' McBride Conferencia', Edimburgo, 1980) ". El diario de laringología y Otología 96 (1): 1 – 23. Doi:10.1017/s0022215100092197. PMID7057076.
- ^ Fienberg R (1955). "Granulomatosis de Pathergic". Soy J. Med. 19 (6): 829 – 31. Doi:10.1016/0002-9343 (55) 90150-9. PMID13275478.
- ^ Mendenhall WM, Olivier KR, Lynch JW Jr, Mendenhall NP (2006). "Lethal midline granuloma nasal natural killer/linfoma de células T". Am J Clin Oncol 29 (2): 202 – 6. Doi:10.1097/01.COC.0000198738.61238.EB. PMID16601443.
- ^ Woywodt A, Matteson EL (2006). "Granulomatosis de Wegener, sondeando el pasado del hombre detrás del epónimo incalculable". Reumatología (Oxford) 45 (10): 1303 – 6. Doi:10.1093/Rheumatology/kel258. PMID16887845.
- ^ Woywodt A, Matteson E (2007). ¿"Deben epónimos abandonar? Sí". BMJ 335 (7617): 424. Doi:10.1136/bmj.39308.342639.ad. PMC1962844. PMID17762033.
Enlaces externos
- Criterios de clasificación por el Colegio estadounidense de Reumatología
- Granulomatosis de Wegener mayor/GPA Grupo de apoyo al paciente
|
||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||